
支原体是一类无细胞壁的原核微生物,其污染具有高隐蔽性、多传播途径、天然耐药等特点,是生物制药、细胞治疗、疫苗生产及高端细胞研究领域中具挑战性的污染物之一。
支原体污染对生产构成的挑战:
无法过滤去除:支原体直径0.13-0.18μm,介于细菌和病毒之间,常规除菌过滤无法清除。
天然耐药:无细胞壁结构,对常用的抗生素(如β- 内酰胺类)具有抗药性。
隐形污染:污染后不浑浊、不产酸,长期潜伏而不被察觉。
法规强制要求:
一旦发生污染,往往导致整批产品报废,并可能干扰细胞库建库、病毒收获等关键生产环节,造成巨大经济损失和生产延误。正因如此,支原体检测成为生物制药、细胞治疗、疫苗生产及高端细胞研究领域质量控制的基石,包括《美国药典》在内的各药典规定,在存在真核细胞的情况下生产的产品的放行必须进行支原体污染检测。

生物梅里埃1小时自动化支原体检测方案
传统支原体检测(培养法+指示细胞法)虽权威可靠,但依赖于细胞培养,检测周期长达28天,难以匹配细胞治疗、基因治疗等先进疗法仅数天的有效期。虽然有作为替代的常规核酸检测(NAT)方法可供选择,获得结果的时间需5-7小时,但是对于操作者仍有一定的要求,并且还需要建立独立的分子实验室。
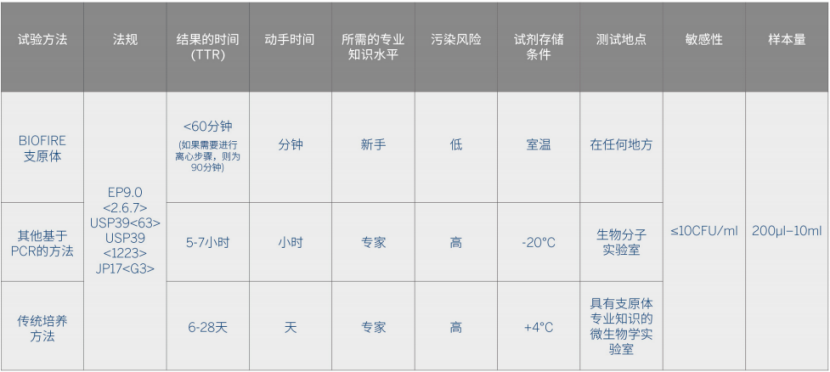
图1:来源生物梅里埃资料
产品推荐
BIOFIRE FILMARRAY 2.O支原体PCR快速检测系统
梅里埃推出了BIOFIRE FILMARRAY 2.O支原体PCR快速检测系统,该系统采用FILMARRAY™ 2.0工业版仪器+封闭PCR检测试剂袋,可检测130多种不同的支原体。
BIOFIRE的科技在于其被称为“口袋分子实验室”的一次性使用的封闭试剂袋,在封闭试剂袋中自动完成细胞裂解、核酸纯化、逆转录及第一和第二阶段巢式PCR等过程,使得整个样本准备非常简便。试剂袋内还包含三步内部质量控制,通过检测从样本提取到扩增检测各步骤,确保结果的可靠性。
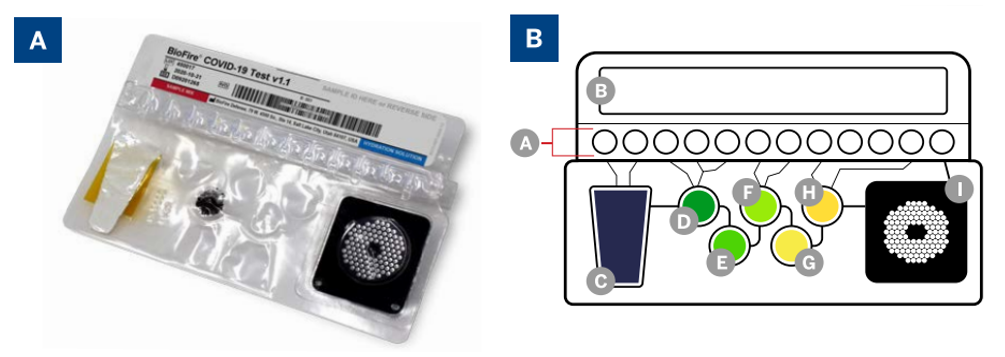
图2:A.BIOFIRE支原体试剂袋。(来源生物梅里埃资料)
B.BIOFIRE支原体试剂袋示意图:(A)装有冻干试剂的装置;(B)活塞-将试剂输送到孔位中;(C)样本溶解和磁珠收集;(D)洗涤;(E)磁珠收集孔位;(F)洗脱;(G)多重PCR孔位;(H)稀释气泡;(I)巢式PCR阵列
BIOFIRE®支原体试剂袋在紧凑型FilmArray 2.0仪器上运行,该仪器可自动执行从细胞裂解到检测分析的所有步骤,在运行开始可在1小时内获得最终结果。FILMARRAY™ 2.0工业版软件符合21 CFR Part 11,1小时内直接报告“检测到支原体”或“未检测到支原体”。
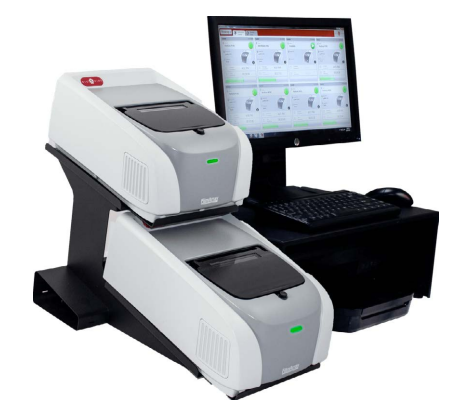
图3:FILMARRAY 2.0工业版仪器执行提取、扩增和检测(宽x深x高=25.4x39.3x16.5cm)。
本系统标配有2台仪器;单台PC可以连接最多8台仪器。(来源生物梅里埃资料)
产品优势
简化培训要求
减少专业知识要求
获得客观的结果
减少人为错误风险/提高数据完整性
无需使用PCR实验室
获得结果只需要1小时,实现检测计划的灵活性
可提供早期污染预警,降低非质量成本
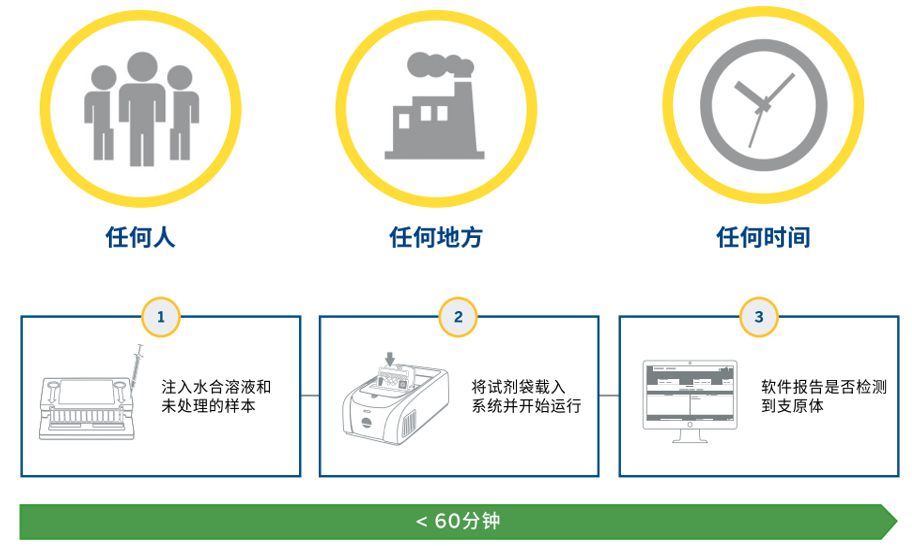
生物梅里埃1小时自动化支原体检测方案,将28天的漫长等待压缩至1小时,同时保证灵敏度与法规合规性,真正实现“快而不疏,准而简便”。
END
关于康成百澳生物
生命科学领域快速消费品及配套服务的专业供应商,总部位于泰州医药城,上海、广州、南京、重庆、成都、苏州、杭州、武汉、济南等地设有分公司及办事处。
产品线涵盖精准医疗、抗体、疫苗、CGT、分子生物学与细胞生物学、常规临床检验、药物筛选、基因组学与蛋白质组学等研究和应用领域,以“技术+产品+服务”的一体化模式服务客户。

©2022-2025 柏澳集 All Rights Reserved. 苏ICP备19039921号-2
建议您使用Chrome、Firefox、Edge、IE10及以上版本和360等主流浏览器浏览本网站。
本网站销售的所有产品均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。
互联网药品信息服务资格证书编号:苏-经营性-2022-0029 、增值电信业务经营许可证:苏B2-20221250 、医疗器械生产(经营)许可证或备案凭证编号:苏泰食药监械经营备20207022号